
L'autre problème du CO2 est l’acidification des océans. L'expérience proposée a pour but d’illustrer le rôle du dioxyde de carbone (CO2) dissous dans l’acidification des océans.
Elle offre aussi l'occasion d'une discussion sur le cycle du carbone : respiration, photosynthèse et répartition entre les différents réservoirs (océan, atmosphère, végétation et sols) du CO2 émis par les activités humaines et en particulier celui issu de la combustion des combustibles fossiles (charbon, pétrole, gaz naturel). Elle s’adresse à des scolaires de niveaux variés et au grand public.
Le matériel
- Des gobelets transparents
- Un kit de test pH
- De l’eau, du vinaigre et de la limonade
- Des craies
- Des pailles
L'expérience
Premiers tests :
Commencer par tester 3 liquides différents comme l’eau, la limonade et le vinaigre. Remplir des gobelets différents puis y mettre quelques gouttes de révélateur pH. La couleur du liquide change révélant ainsi l’acidité du liquide testé.
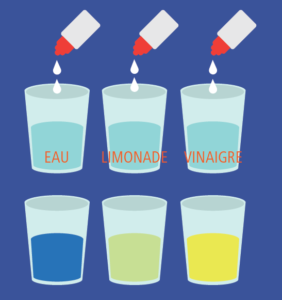
© IPSL - Julie Sistenich
L’expérience 1 : effet du CO2 sur l’acidité de l’eau
Verser de l’eau dans un gobelet puis quelques gouttes de révélateur pH. Souffler pendant plusieurs minutes à l’aide d’une paille sans aspirer ! Observer le changement de couleur pH : l’eau s’est acidifiée. C’est parce que le CO2 émis lorsque nous respirons se dissout dans l’eau et l’acidifie. Laisser reposer quelques minutes : on constate que l’eau redevient neutre. C’est parce que le CO2 solubilisé dans l’eau est reparti dans l’atmosphère.

© IPSL - Julie Sistenich
L’expérience 2 : effet de l’acidité de l’eau sur le calcaire
Prendre deux gobelets dont l’un contient de l’eau et l’autre du vinaigre. Plonger une craie dans chacun d’eux. On constate que la craie est effervescente dans le vinaigre. C’est parce que l’acidité attaque le calcaire et le dissout.
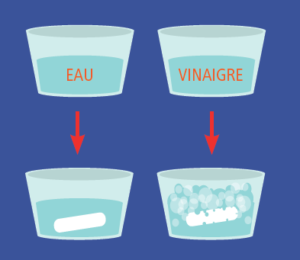
© IPSL - Julie Sistenich
Pour aller plus loin
D’où vient le dioxyde de carbone (CO2) ?
Le CO2 est un des principaux gaz incriminés dans le réchauffement climatique, à cause de son rôle dans l’effet de serre. Sa quantité a augmenté significativement depuis la révolution industrielle. En effet, les activités humaines produisent du CO2 : en brûlant, la matière organique comme le charbon, le pétrole ou l’essence libère le carbone qu’elle contient sous forme de CO2. Du CO2 est aussi produit naturellement par les différents organismes. Par exemple, en respirant, les animaux libèrent du CO2. De même, les micro-organismes libèrent du CO2 en fermentant. Le volcanisme émet aussi du CO2, en quantité toutefois infime par rapport aux autres sources.
Que devient le CO2 ?
Tout le CO2 produit par les activités humaines ne s’accumule pas dans l’atmosphère : environ un quart de l’excès de CO₂ est absorbé par les végétaux au cours de la photosynthèse. Un autre quart est absorbé par l’océan après s’y être dissous. La moitié restante s’accumule dans l’atmosphère. Quand le CO2 se dissout dans l’océan, l’océan s’acidifie. C’est ce qu’on constate dans l’expérience 1. Ceci comporte des risques pour les êtres vivants comportant du calcaire, comme les coraux. L’acidité attaque en effet le calcaire, comme le montre l’expérience 2.
Merci à Alain Mazaud, Aliénor Lavergne, Camille Risi et Olivier Boucher.
À lire : Quelques expériences simples sur l’autre problème du CO2 : l’acidification des océans. A. Mazaud La Météorologie - n° 90 - août 2015.






